تسمح النظرية الحركية الجزيئية ، من خلال تحليل السلوك المجهري للنظام واستخدام طرق الميكانيكا الإحصائية ، بالحصول على الخصائص العيانية الهامة للنظام الديناميكي الحراري. إحدى الخصائص المجهرية ، التي ترتبط بدرجة حرارة النظام ، هي متوسط السرعة المربعة لجزيئات الغاز. نعطي الصيغة لها ونعتبرها في المقال.
الغاز المثالي
نلاحظ على الفور أن صيغة متوسط السرعة التربيعية لجزيئات الغاز ستعطى خصيصًا للغاز المثالي. تحته ، في الفيزياء ، يُنظر إلى مثل هذا النظام متعدد الجسيمات حيث لا تتفاعل الجسيمات (الذرات والجزيئات) مع بعضها البعض (تتجاوز طاقتها الحركية الطاقة الكامنة للتفاعل بعدة أوامر من حيث الحجم) وليس لها أبعاد ، أي أنها نقاط ذات كتلة محدودة (المسافة بين الجسيمات عدة مرات من حيث الحجم أكبر من حجمها.خطي).
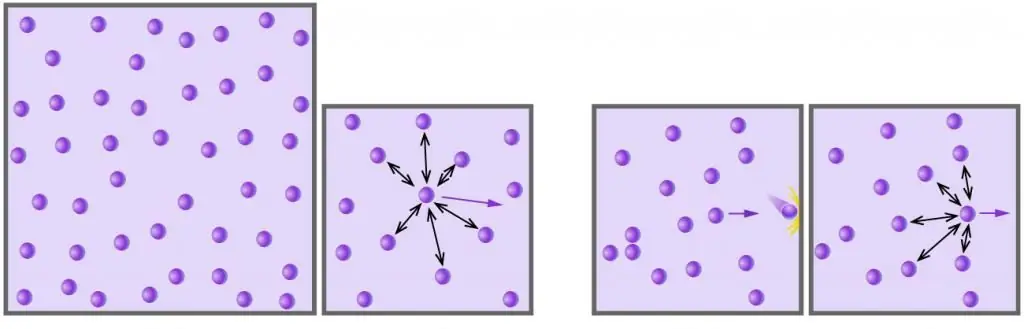
أي غاز يتكون من جزيئات أو ذرات متعادلة كيميائيًا ، ويكون تحت ضغط منخفض ودرجة حرارة عالية ، يمكن اعتباره مثاليًا. على سبيل المثال ، يعد الهواء غازًا مثاليًا ، لكن بخار الماء لم يعد كذلك (تعمل الروابط الهيدروجينية القوية بين جزيئات الماء).
النظرية الحركية الجزيئية (MKT)

دراسة غاز مثالي في إطار MKT ، يجب الانتباه إلى عمليتين مهمتين:
- الغاز يخلق ضغطًا عن طريق الانتقال إلى جدران الوعاء الذي يحتويه ، الزخم عندما تصطدم الجزيئات والذرات بها. مثل هذه الاصطدامات مرنة تمامًا.
- جزيئات وذرات الغاز تتحرك بشكل عشوائي في جميع الاتجاهات بسرعات مختلفة ، ويتبع توزيعها إحصائيات ماكسويل بولتزمان. احتمال الاصطدام بين الجسيمات منخفض للغاية ، بسبب حجمها الضئيل والمسافات الكبيرة بينها.
على الرغم من أن السرعات الفردية لجزيئات الغاز مختلفة تمامًا عن بعضها البعض ، فإن متوسط قيمة هذه القيمة يظل ثابتًا بمرور الوقت إذا لم تكن هناك تأثيرات خارجية على النظام. يمكن الحصول على صيغة متوسط السرعة المربعة لجزيئات الغاز من خلال النظر في العلاقة بين الطاقة الحركية ودرجة الحرارة. سنتعامل مع هذه المسألة في الفقرة التالية من المقال
اشتقاق معادلة السرعة المتوسطة التربيعية لجزيئات الغاز المثالية
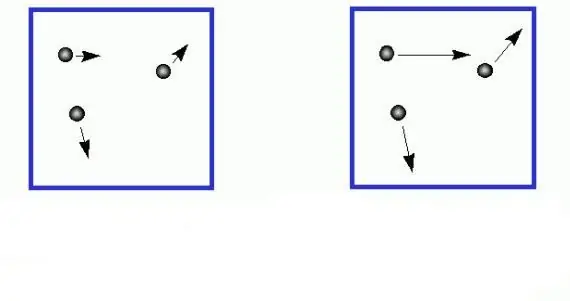
يعرف كل طالب من المقرر العام للفيزياء أن الطاقة الحركية للحركة الانتقالية لجسم كتلته m تُحسب على النحو التالي:
Ek=mv2/ 2
حيث v هي السرعة الخطية. من ناحية أخرى ، يمكن أيضًا تحديد الطاقة الحركية للجسيم من حيث درجة الحرارة المطلقة T ، باستخدام عامل التحويل kB(ثابت بولتزمان). نظرًا لأن مساحتنا ثلاثية الأبعاد ، يتم حساب Ekعلى النحو التالي:
Ek=3/2kB T.
أي ما يعادل كلا من المساواة والتعبير عن v منهما ، نحصل على صيغة لمتوسط سرعة الغاز المثالي التربيعي:
mv2/ 2=3/2kB T=>
v=√ (3kB T / م).
في هذه الصيغة ، م - كتلة جسيم الغاز. قيمته غير ملائمة للاستخدام في الحسابات العملية ، لأنها صغيرة (≈ 10-27kg). لتجنب هذا الإزعاج ، دعونا نتذكر ثابت الغاز العام R والكتلة المولية M. ويرتبط الثابت R مع kBبالمساواة:
كB=R / NA.
يتم تحديد قيمة M على النحو التالي:
M=مNA.
مع الأخذ في الاعتبار كلا المساواة ، نحصل على التعبير التالي لسرعة الجذر التربيعي للجزيئات:
v=√ (3RT / M).
وهكذا ، فإن متوسط السرعة التربيعية لجزيئات الغاز يتناسب طرديا مع الجذر التربيعي لدرجة الحرارة المطلقة ويتناسب عكسيا مع الجذر التربيعي للكتلة المولية.
مثال على حل المشكلات
يعلم الجميع أن الهواء الذي نتنفسه يتكون من 99٪ من النيتروجين والأكسجين. من الضروري تحديد الاختلافات في متوسط سرعات الجزيئات N2و O2عند درجة حرارة 15سC.

سيتم حل هذه المشكلة بالتتابع. أولاً ، نترجم درجة الحرارة إلى وحدات مطلقة ، لدينا:
T=273 ، 15 + 15=288 ، 15 ك.
الآن اكتب الكتل المولية لكل جزيء قيد الدراسة:
MN2=0.028 كجم / مول ؛
MO2=0.032 كجم / مول.
نظرًا لاختلاف قيم الكتل المولية اختلافًا طفيفًا ، فإن متوسط سرعاتها عند نفس درجة الحرارة يجب أن يكون قريبًا أيضًا. باستخدام صيغة v ، نحصل على القيم التالية لجزيئات النيتروجين والأكسجين:
v (N2)=√ (38 ، 314288 ، 15/0 ، 028)=506.6 م / ث ؛
v (O2)=√ (38 ، 314288 ، 15/0 ، 032)=473.9 م / ث.
لأن جزيئات النيتروجين أخف قليلاً من جزيئات الأكسجين ، فإنها تتحرك بشكل أسرع. متوسط فرق السرعة هو:
v (N2) - v (O2)=506.6 - 473.9=32.7 م / ث.
القيمة الناتجة هي فقط 6.5٪ من متوسط سرعة جزيئات النيتروجين. نلفت الانتباه إلى السرعات العالية للجزيئات في الغازات ، حتى في درجات الحرارة المنخفضة.






