يصعب دراسة الحالة ثلاثية الأبعاد للماء السائل ، ولكن تم تعلم الكثير من خلال تحليل بنية بلورات الجليد. أربع ذرات أكسجين متجاورة تتفاعل مع الهيدروجين تحتل رؤوس رباعي الوجوه (رباعي=أربعة ، هيدرون=مستوي). يقدر متوسط الطاقة المطلوبة لكسر مثل هذه الرابطة في الجليد بـ 23 كيلو جول / مول-1.

إن قدرة جزيئات الماء على تكوين عدد معين من سلاسل الهيدروجين ، بالإضافة إلى قوة معينة ، تخلق نقطة انصهار عالية بشكل غير عادي. عندما يذوب ، يتم تثبيته بالماء السائل ، هيكله غير منتظم. معظم الروابط الهيدروجينية مشوهة. يتطلب الأمر كمية كبيرة من الطاقة على شكل حرارة لكسر الشبكة البلورية للجليد المرتبط بالهيدروجين.
ملامح مظهر الجليد
يتساءل العديد من السكان عن نوع الجليد الشبكي البلوري. ضروريوتجدر الإشارة إلى أن كثافة معظم المواد تزداد أثناء التجميد ، عندما تتباطأ الحركات الجزيئية وتتشكل بلورات معبأة بكثافة. تزداد كثافة الماء أيضًا عندما يبرد إلى حد أقصى عند 4 درجات مئوية (277 كلفن). ثم ، عندما تنخفض درجة الحرارة عن هذه القيمة ، فإنها تتسع.
ترجع هذه الزيادة إلى تكوين بلورة جليدية مفتوحة مرتبطة بالهيدروجين بشبكتها وكثافتها المنخفضة ، حيث يرتبط كل جزيء ماء بشكل صارم بالعنصر أعلاه وأربع قيم أخرى ، بينما يتحرك بسرعة كافية لديها كتلة أكبر. منذ حدوث هذا الإجراء ، يتجمد السائل من أعلى إلى أسفل. هذا له نتائج بيولوجية مهمة ، ونتيجة لذلك فإن طبقة الجليد على البركة تعزل الكائنات الحية بعيدًا عن البرودة الشديدة. بالإضافة إلى ذلك ، ترتبط خاصيتان إضافيتان للماء بخصائصه الهيدروجينية: الحرارة النوعية والتبخر.
وصف مفصل للهياكل
المعيار الأول هو المقدار المطلوب لرفع درجة حرارة 1 جرام من مادة بمقدار 1 درجة مئوية. يتطلب رفع درجات الماء قدرًا كبيرًا نسبيًا من الحرارة لأن كل جزيء متورط في العديد من الروابط الهيدروجينية التي يجب كسرها لزيادة الطاقة الحركية. بالمناسبة ، فإن وفرة H2O في خلايا وأنسجة جميع الكائنات متعددة الخلايا الكبيرة تعني تقليل تقلبات درجة الحرارة داخل الخلايا. هذه الميزة حاسمة ، حيث أن معدل معظم التفاعلات الكيميائية الحيويةحساسة.
كما أن حرارة تبخر الماء أعلى بكثير من حرارة العديد من السوائل الأخرى. يلزم قدر كبير من الحرارة لتحويل هذا الجسم إلى غاز ، لأنه يجب كسر الروابط الهيدروجينية حتى تنفصل جزيئات الماء عن بعضها البعض وتدخل في المرحلة المذكورة. الأجسام القابلة للتغيير هي ثنائيات أقطاب دائمة ويمكن أن تتفاعل مع مركبات أخرى مماثلة وتلك التي تتأين وتذوب.
المواد الأخرى المذكورة أعلاه يمكن أن تتلامس فقط في حالة وجود قطبية. هذا المركب هو الذي يشارك في بنية هذه العناصر. بالإضافة إلى ذلك ، يمكن محاذاة حول هذه الجسيمات المتكونة من الإلكتروليتات ، بحيث يتم توجيه ذرات الأكسجين السالبة لجزيئات الماء إلى الكاتيونات ، ويتم توجيه الأيونات الموجبة وذرات الهيدروجين إلى الأنيونات.
في المواد الصلبة ، كقاعدة عامة ، تتشكل المشابك البلورية الجزيئية والذرية. بمعنى ، إذا تم بناء اليود بطريقة تحتوي على I2 ،، فعندئذٍ في ثاني أكسيد الكربون الصلب ، أي في الجليد الجاف ، تكون جزيئات ثاني أكسيد الكربون2 تقع في العقد الشبكية البلورية. عند التفاعل مع مواد مماثلة ، يكون للجليد شبكة بلورية أيونية. الجرافيت ، على سبيل المثال ، الذي له هيكل ذري يعتمد على الكربون ، غير قادر على تغييره ، تمامًا مثل الماس.
ماذا يحدث عندما تذوب بلورة ملح الطعام في الماء: تنجذب الجزيئات القطبية إلى العناصر المشحونة في البلورة ، مما يؤدي إلى تكوين جزيئات متشابهة من الصوديوم والكلوريد على سطحها ، مما ينتج عنه هذه الأجسامتنفصل عن بعضها ، وتبدأ في الذوبان. من هنا يمكن ملاحظة أن الجليد به شبكة بلورية ذات رابطة أيونية. يجذب كل Na + المذاب الأطراف السلبية للعديد من جزيئات الماء ، بينما كل Cl المذاب - يجذب النهايات الإيجابية. الغلاف المحيط بكل أيون يسمى كرة الهروب وعادة ما يحتوي على عدة طبقات من جزيئات المذيب.
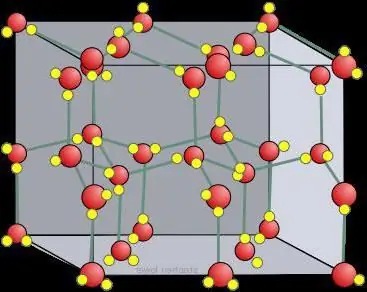
شعرية الكريستال الجليد الجاف
يقال أن المتغيرات أو الأيون المحاط بالعناصر مكبريت. عندما يكون المذيب ماء ، فإن هذه الجسيمات تكون رطبة. وبالتالي ، فإن أي جزيء قطبي يميل إلى الذوبان بواسطة عناصر الجسم السائل. في الجليد الجاف ، يشكل نوع الشبكة البلورية روابط ذرية في حالة التجمع ، والتي لا تتغير. شيء آخر هو الثلج البلوري (الماء المجمد). يجب أن تكون المركبات العضوية الأيونية مثل الكربوكسيلاز والأمينات البروتونية قابلة للذوبان في مجموعات الهيدروكسيل والكربونيل. الجسيمات الموجودة في مثل هذه الهياكل تتحرك بين الجزيئات ، وتشكل أنظمتها القطبية روابط هيدروجينية مع هذا الجسم.
بالطبع ، يؤثر عدد المجموعات الأخيرة المشار إليها في الجزيء على قابليته للذوبان ، والذي يعتمد أيضًا على تفاعل الهياكل المختلفة في العنصر: على سبيل المثال ، الكحولات أحادية وثنائية وثلاثية الكربون قابلة للامتزاج مع الماء ، لكن الهيدروكربونات الأكبر التي تحتوي على مركبات هيدروكسيل مفردة تكون أقل تمييعًا في السوائل.
سداسي Ih مشابه في الشكل لـشعرية الكريستال الذرية. بالنسبة للجليد وكل الثلج الطبيعي على الأرض ، يبدو تمامًا مثل هذا. يتضح هذا من خلال تناظر الشبكة البلورية للجليد ، التي تنمو من بخار الماء (أي ، رقاقات الثلج). إنه موجود في المجموعة الفضائية P 63 / مم من 194 ؛ D 6h ، فئة Laue 6 / مم ؛ على غرار β- ، الذي يحتوي على مضاعفات 6 محاور حلزونية (الدوران حول بالإضافة إلى التحول على طوله). إنه ذو بنية منخفضة الكثافة مفتوحة إلى حد ما حيث تكون الكفاءة منخفضة (~ 1/3) مقارنة بالبنى المكعبة البسيطة (~ 1/2) أو الهياكل المكعبة المتمركزة على الوجه (~ 3/4).
بالمقارنة مع الجليد العادي ، فإن الشبكة البلورية للثلج الجاف ، المرتبطة بجزيئات CO2، ثابتة ولا تتغير إلا عندما تتحلل الذرات.
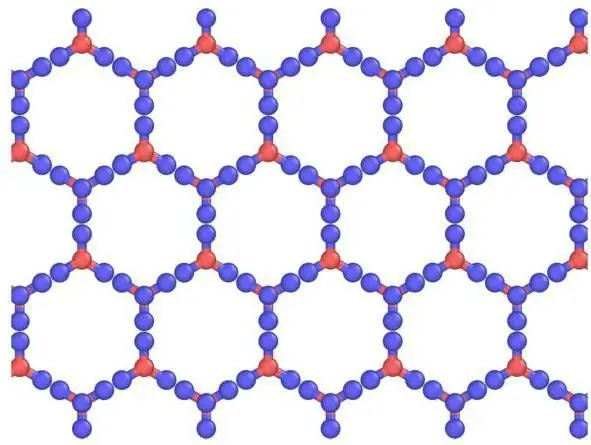
وصف الشبكات وعناصرها
يمكن اعتبار البلورات على أنها نماذج بلورية ، تتكون من صفائح موضوعة واحدة فوق الأخرى. يتم ترتيب الرابطة الهيدروجينية ، بينما هي في الواقع عشوائية ، حيث يمكن للبروتونات أن تتحرك بين جزيئات الماء (الجليد) عند درجات حرارة أعلى من حوالي 5 كلفن. يتم تعزيز ذلك من خلال تشتت النيوترونات ، مما يدل على كثافة تشتتها في منتصف الطريق بين ذرات الأكسجين ، مما يشير إلى التوطين والحركة المنسقة. يوجد هنا تشابه بين الجليد وشبكة بلورية جزيئية ذرية.
الجزيئات لها ترتيب متعرج لسلسلة الهيدروجينفيما يتعلق بجيرانها الثلاثة في الطائرة. العنصر الرابع له ترتيب رابطة هيدروجين مكسوف. يوجد انحراف طفيف عن التناظر السداسي المثالي ، حيث تكون خلية الوحدة أقصر بنسبة 0.3٪ في اتجاه هذه السلسلة. تختبر جميع الجزيئات نفس البيئات الجزيئية. هناك مساحة كافية داخل كل "صندوق" لحمل جزيئات الماء الخلالي. على الرغم من عدم أخذها في الاعتبار بشكل عام ، فقد تم اكتشافها مؤخرًا بشكل فعال عن طريق حيود النيوترون للشبكة البلورية المسحوقة للجليد.
تغيير المواد
يحتوي الجسم السداسي على نقاط ثلاثية مع الماء السائل والغازي 0.01 درجة مئوية ، 612 باسكال ، عناصر صلبة - ثلاثة -21.985 درجة مئوية ، 209.9 ميجا باسكال ، أحد عشر واثنان -199.8 درجة مئوية ، 70 ميجا باسكال ، وكذلك - 34.7 درجة مئوية ، 212.9 ميجا باسكال. ثابت العزل الكهربائي للثلج السداسي هو 97.5.
يتم إعطاء منحنى الانصهار لهذا العنصر بواسطة MPa. تتوفر معادلات الحالة ، بالإضافة إلى ذلك ، بعض التفاوتات البسيطة المتعلقة بالتغير في الخصائص الفيزيائية لدرجة حرارة الجليد السداسي ومعلقاته المائية. تتقلب الصلابة مع درجات ترتفع من أو تحت الجبس (≦ 2) عند 0 درجة مئوية إلى الفلسبار (6 موس) عند -80 درجة مئوية ، وهو تغير كبير بشكل غير طبيعي في الصلابة المطلقة (> 24 مرة).
تشكل الشبكة البلورية السداسية للجليد صفائح وأعمدة سداسية ، حيث تكون الوجوه العلوية والسفلية هي المستويات القاعدية {0 0 0 1} مع محتوى حراري يبلغ 5.57 ميكرولتر سم -2، والأجزاء الجانبية المكافئة الأخرى تسمى أجزاء من المنشور {1 0 -1 0} مع 5 ، 94µJ سم-2. الأسطح الثانوية {1 1 -2 0} 6.90 ΜJ ˣ cm-2يمكن تشكيلها على طول المستويات التي تشكلها جوانب الهياكل.
يظهر هذا الهيكل انخفاضًا غير طبيعي في التوصيل الحراري مع زيادة الضغط (بالإضافة إلى الجليد المكعب وغير المتبلور منخفض الكثافة) ، ولكنه يختلف عن معظم البلورات. هذا بسبب التغيير في رابطة الهيدروجين ، مما يقلل من السرعة العرضية للصوت في الشبكة البلورية للثلج والماء.
هناك طرق تصف كيفية تحضير عينات بلورية كبيرة وأي سطح جليدي مرغوب فيه. من المفترض أن تكون الرابطة الهيدروجينية على سطح الجسم السداسي قيد الدراسة أكثر ترتيبًا من داخل نظام الكتلة. أظهر التحليل الطيفي المتغير مع توليد تردد الطور الشبكي أن هناك عدم تناسق هيكلي بين الطبقتين العلويتين (L1 و L2) في سلسلة H O تحت السطحية للسطح القاعدي للجليد السداسي. الروابط الهيدروجينية المعتمدة في الطبقات العليا من السداسيات (L1 O ··· HO L2) أقوى من تلك المقبولة في الطبقة الثانية للتراكم العلوي (L1 OH ··· O L2). تتوفر هياكل الجليد سداسية التفاعلية.
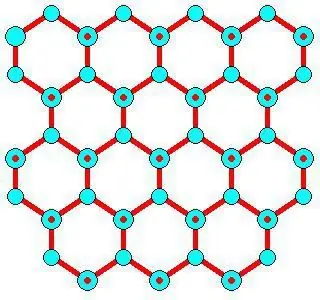
ميزات التطوير
الحد الأدنى لعدد جزيئات الماء اللازمة لتشكيل الجليد هو حوالي 275 ± 25 ، كما هو الحال بالنسبة لمجموعة كاملة مكونة من عشري الوجوه مكونة من 280. يحدث التكوين بمعدل 1010عند واجهة الهواء والماء وليس في المياه السائبة. يعتمد نمو بلورات الجليد على معدلات نمو مختلفة مختلفةالطاقات. يجب حماية المياه من التجمد عند حفظ العينات البيولوجية والأغذية والأعضاء بالتبريد.
يتم تحقيق ذلك عادةً من خلال معدلات التبريد السريعة ، واستخدام عينات صغيرة وحافظة التجميد ، وزيادة الضغط لتكوين الجليد ومنع تلف الخلايا. تزداد الطاقة الحرة للجليد / السائل من ~ 30 مللي جول / م2عند الضغط الجوي إلى 40 مللي جول / م-2عند 200 ميجا باسكال ، مما يشير سبب حدوث هذا التأثير
ما هو نوع الشبكة البلورية المميزة للجليد
بدلاً من ذلك ، يمكن أن تنمو بشكل أسرع من أسطح المنشور (S2) ، على السطح المضطرب عشوائيًا للبحيرات سريعة التجمد أو الاهتزاز. النمو من الوجوه {1 1 -2 0} هو نفسه على الأقل ، لكنه يحولها إلى قواعد منشور. تم فحص البيانات المتعلقة بتطوير بلورات الثلج بشكل كامل. تعتمد معدلات النمو النسبية لعناصر الوجوه المختلفة على القدرة على تكوين درجة كبيرة من ترطيب المفاصل. تحدد درجة حرارة (منخفضة) المياه المحيطة درجة التفرع في بلورة الجليد. نمو الجسيمات مقيد بمعدل الانتشار بدرجة منخفضة من التبريد الفائق ، أي <2 درجة مئوية ، مما أدى إلى المزيد منها.

لكنها محدودة بسبب حركية التنمية عند مستويات أعلى من الاكتئاب تبلغ >4 درجة مئوية ، مما يؤدي إلى نمو الإبرة. يشبه هذا الشكل هيكل الجليد الجاف (له شبكة بلورية ذات هيكل سداسي) ، متنوعخصائص تطور السطح ودرجة حرارة المياه المحيطة (فائقة البرودة) والتي هي خلف الأشكال المسطحة لثلج الثلج.
تكوين الجليد في الغلاف الجوي يؤثر تأثيرا عميقا في تكوين الغيوم وخصائصها. الفلسبار ، الموجود في الغبار الصحراوي الذي يدخل الغلاف الجوي بملايين الأطنان سنويًا ، من العناصر المهمة. أظهرت عمليات المحاكاة الحاسوبية أن هذا يرجع إلى تنوي الطائرات البلورية الجليدية المنشورية على سطوح عالية الطاقة.
بعض العناصر والمشابك الأخرى
لا يمكن تضمين المواد المذابة (باستثناء الهيليوم والهيدروجين الصغير جدًا ، والتي يمكن أن تدخل الفجوات) في هيكل Ih عند الضغط الجوي ، ولكن يتم إجبارها على الخروج إلى السطح أو الطبقة غير المتبلورة بين جزيئات الجسم الجريزوفولفين. هناك بعض العناصر الأخرى في المواقع الشبكية للجليد الجاف: أيونات تشوتروبيك مثل NH4+و Cl- التي يتم تضمينها في تجميد سائل أخف من غيرها من الأنواع الكونية مثل Na+و SO42-، لذا لا يمكن إزالتها نظرًا لكونها تشكل طبقة رقيقة من السائل المتبقي بين البلورات. يمكن أن يؤدي ذلك إلى الشحن الكهربائي للسطح بسبب تفكك المياه السطحية التي توازن الشحنات المتبقية (والتي يمكن أن تؤدي أيضًا إلى إشعاع مغناطيسي) وتغير في الرقم الهيدروجيني للأغشية السائلة المتبقية ، على سبيل المثال NH42SO4يصبح أكثر حمضية ويصبح كلوريد الصوديوم أكثر أساسية.
عمودي على الوجوهشبكة بلورية من الجليد تظهر الطبقة التالية متصلة (مع ذرات O باللون الأسود). وتتميز بسطح قاعدي ينمو ببطء {0 0 0 1} ، حيث يتم ربط جزيئات الماء المعزولة فقط. سطح منشور {1 0-1 0} سريع النمو حيث يمكن لأزواج من الجسيمات الملتصقة حديثًا أن تترابط مع بعضها البعض باستخدام الهيدروجين (رابطة هيدروجينية واحدة / جزيئين من عنصر). الوجه الأسرع نموًا هو {1 1 -2 0} (موشوري ثانوي) ، حيث يمكن أن تتفاعل سلاسل الجسيمات الملتصقة حديثًا مع بعضها البعض عن طريق الرابطة الهيدروجينية. أحد جزيئات السلاسل / العنصر هو شكل يشكل حواف تقسم وتشجع التحول إلى وجهين من المنشور.
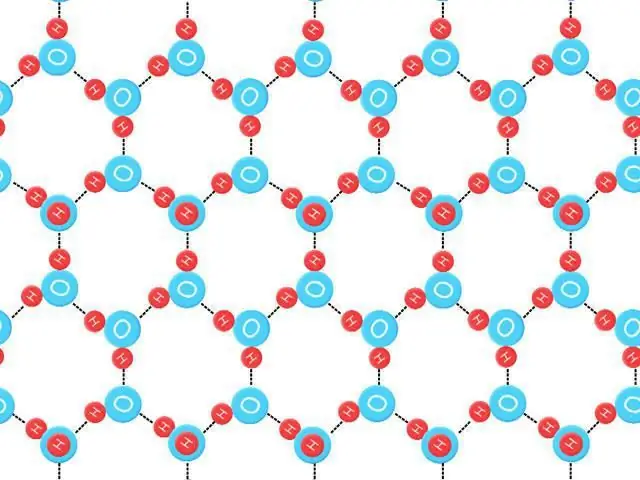
إنتروبيا نقطة الصفر
يمكن تعريفه على أنه S0=kBˣ Ln (NE0) ، حيث k B هو ثابت بولتزمان ، NEهو عدد التكوينات عند الطاقة E ، و E0 هي أقل طاقة. هذه القيمة لانتروبيا الجليد السداسي عند صفر كلفن لا تنتهك القانون الثالث للديناميكا الحرارية "إن إنتروبيا بلورة مثالية عند الصفر المطلق هي صفر تمامًا" ، نظرًا لأن هذه العناصر والجسيمات ليست مثالية ، فقد اختلت الروابط الهيدروجينية.
في هذا الجسم ، تكون الرابطة الهيدروجينية عشوائية وتتغير بسرعة. هذه الهياكل ليست متساوية تمامًا في الطاقة ، ولكنها تمتد إلى عدد كبير جدًا من الحالات القريبة بقوة ، تخضع لـ "قواعد الجليد". إنتروبيا نقطة الصفر هو الاضطراب الذي سيبقى حتى لو تم تبريد المادة إلى درجة مطلقةصفر (0 ك=-273 ، 15 درجة مئوية). يولد ارتباكًا تجريبيًا للجليد السداسي 3 ، 41 (± 0 ، 2) ˣ مول-1ˣ K-1. من الناحية النظرية ، سيكون من الممكن حساب الانتروبيا الصفرية لبلورات الجليد المعروفة بدقة أكبر بكثير (إهمال العيوب وانتشار مستوى الطاقة) من تحديدها بشكل تجريبي.
العلماء وعملهم في هذا المجال
يمكن تعريفه على أنه S0=kBˣ Ln (NE0) ، حيث k B هو ثابت بولتزمان ، NEهو عدد التكوينات عند الطاقة E ، و E0 هي أقل طاقة. هذه القيمة لانتروبيا الجليد السداسي عند صفر كلفن لا تنتهك القانون الثالث للديناميكا الحرارية "إن إنتروبيا بلورة مثالية عند الصفر المطلق هي صفر تمامًا" ، نظرًا لأن هذه العناصر والجسيمات ليست مثالية ، فقد اختلت الروابط الهيدروجينية.
في هذا الجسم ، تكون الرابطة الهيدروجينية عشوائية وتتغير بسرعة. هذه الهياكل ليست متساوية تمامًا في الطاقة ، ولكنها تمتد إلى عدد كبير جدًا من الحالات القريبة بقوة ، تخضع لـ "قواعد الجليد". إنتروبيا نقطة الصفر هو الاضطراب الذي سيبقى حتى لو تم تبريد المادة إلى الصفر المطلق (0 ك=-273.15 درجة مئوية). يولد ارتباكًا تجريبيًا للجليد السداسي 3 ، 41 (± 0 ، 2) ˣ مول-1ˣ K-1. من الناحية النظرية ، سيكون من الممكن حساب الانتروبيا الصفرية لبلورات الجليد المعروفة بدقة أكبر بكثير (إهمال العيوب وانتشار مستوى الطاقة) من تحديدها بشكل تجريبي.

على الرغم من عدم ترتيب ترتيب البروتونات في الجليد الكتلي ، فمن المحتمل أن السطح يفضل ترتيب هذه الجسيمات في شكل نطاقات من ذرات H وأزواج O- مفردة (إنتروبيا صفرية مع روابط هيدروجينية مرتبة). تم العثور على اضطراب نقطة الصفر ZPE و J ˣ mol-1ˣ K-1وغيرها. مما سبق ، من الواضح والمفهوم ما هي أنواع المشابك البلورية التي تتميز بها الجليد.






